Nach dem grünen Licht der EU-Arzneimittelbehörde für den Impfstoff von Biontech/Pfizer, hat die EU-Kommission die Zulassung bestätigt. Erste Impfungen zu Jahreswechsel in Österreich sind dadurch möglich.
Fast zehn Monate nach Ausbruch der Corona-Pandemie in Europa kann es in der Europäischen Union mit den Impfungen losgehen. Die EU-Kommission erteilte dem Impfstoff des Mainzer Unternehmens Biontech und seines US-Partners Pfizer am Montag die Marktzulassung. "Heute fügen wir dem Kampf gegen Covid-19 ein wichtiges Kapitel hinzu", sagte Kommissionspräsidentin Ursula von der Leyen in Brüssel.
Zuvor hatte die Europäische Arzneimittel-Agentur (EMA) grünes Licht für die Zulassung gegeben. Die Zustimmung der Kommission galt daher als reine Formsache. Die Zulassung sei ein "Meilenstein", sagte die EMA am Montag in Amsterdam. "Das ist wirklich eine historische wissenschaftliche Leistung", sagte EMA-Direktorin Emer Cooke. Außerdem warnte sie: "Wir haben noch nicht den Wendepunkt der Pandemie erreicht."
Der Impfstoff ist bereits unter anderem in Großbritannien, den USA und Kanada zugelassen. Er hat nach Angaben der Hersteller Pfizer und Biontech eine Wirksamkeit von rund 95 Prozent und wird für Personen ab 16 Jahre empfohlen. Außerhalb Europas haben schon die USA und Kanada mit Massenimpfungen mit dem Mittel begonnen.
Die EMA rechnet damit, dass der Impfstoff der Firmen Pfizer und Biontech auch gegen die neu aufgetretene Coronavirus-Variante wirksam ist. "Zu diesem Zeitpunkt gibt es keinen Beweis für die Annahme, dass der Impfstoff nicht gegen die neue Variante wirken könnte", sagte EMA-Direktorin Cooke. Über die neue Virus-Variante müssten aber noch mehr Informationen gesammelt werden.
Mögliche Nebenwirkungen werden geprüft
Die Experten der EMA hatten bereits seit Wochen die Daten und Resultate der klinischen Tests der Hersteller geprüft. Bei einer bedingten Zulassung ist der Hersteller verpflichtet, auch danach noch Daten etwa zur Langzeitwirkung an die EMA zu übermitteln. Auch Angaben zu möglichen Nebenwirkungen werden weiterhin geprüft. Voraussichtlich am 6. Jänner will die EMA auch den Weg frei machen für die Zulassung des zweiten Impfstoffes, dem Präparat vom US-Konzern Moderna.
In den EU-Staaten, also auch in Österreich, sollen die ersten Dosen am kommenden Sonntag (27. Dezember) gespritzt werden. Bis dahin soll das deutsche bundeseigene Paul-Ehrlich-Institut die Impfchargen prüfen und freigeben. Bundeskanzler Sebastian Kurz (ÖVP) begrüßte die Zulassung des ersten Impfstoffes in einer Stellungnahme uns sprach von einem "erfreulichen Tag nach zehn Monaten harten Kampfes gegen die Corona-Pandemie." Gesundheitsminister Rudolf Anschober (Grüne) sprach von einer "Wende im Kampf gegen die Pandemie".
Die Auslieferung der ersten Dosen soll so schnell wie möglich geschehen, Österreich erhält zunächst 10.000 Dosen, zwei Impfungen sind pro Person erforderlich. Gestartet wird mit Impfungen für Menschen in Alten- und Pflegeheimen, für das Gesundheitspersonal und in Hochrisikogruppen. Im ersten Quartal erhält Österreich von Biontech/Pfizer 900.000 Impfdosen. Im Dezember und Jänner sind es 240.825 Dosen, im Februar folgen 331.500 und im März 375.375. Somit können im ersten Quartal in Österreich rund 450.000 Menschen geimpft werden.
Biontech bereit für Auslieferung
Die Hersteller Biontech und Pfizer stehen nach eigenen Angaben in den Startlöchern: "Wir sind bereit, mit der Auslieferung der ersten Impfstoffdosen in der EU zu beginnen, sobald wir grünes Licht erhalten", sagte Biontech-Chef und Mitgründer Ugur Sahin am Montag vor der Entscheidung der EU-Kommission.
Die Experten bekräftigten, dass bei der Prüfung der Daten keinerlei Abstriche bei der Sicherheit gemacht worden waren. Es sei klar, dass es Sorgen wegen der Geschwindigkeit der Zulassung gebe, sagte Harald Enzmann, der Vorsitzende des deutschen Ausschusses für Humanarzneimittel. Aber: "Die analysierten Daten entsprechen den Standards der Verlässlichkeit und Qualität." Nicht zuletzt sei es einer der größten Impfstofftests der Geschichte gewesen.
Wie wirkt der Impfstoff?
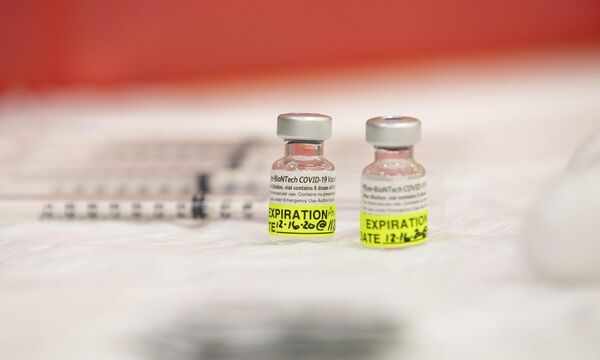
Bei dem Mittel von Biontech und Pfizer handelt es sich um einen sogenannten mRNA-Impfstoff. Bisher wurde noch kein Impfstoff dieser Art für den Menschen zugelassen. Der Unterschied zu herkömmlichen Impfstoffen: Er enthält keine abgeschwächten oder abgetöteten Viren, sondern lediglich die Bauanleitung für einen Bestandteil des Covid-19-Erregers, genauer gesagt für ein Eiweiß der Virusoberfläche.
Die Bauanleitung besteht aus dem Molekül mRNA. Auf ihrer Grundlage stellen die Körperzellen das Virusprotein her. Gegen dieses entwickelt der Körper dann seine Immunantwort. Bei späterem Kontakt mit dem Erreger erkennt das Immunsystem das Protein wieder und kann das Virus schnell gezielt bekämpfen. Weil der Impfstoff eben nur die Information für einen einzelnen Bestandteil des Virus enthält, besteht keine Gefahr, dass sich nach der Impfung Viren im Körper ausbreiten.
Wovor schützt der Impfstoff nachweislich?
"Die Impfstoffversuche zeigen, dass Menschen nicht mehr symptomatisch erkranken", sagt Andreas Podbielski, Direktor des Instituts für Medizinische Mikrobiologie, Virologie und Hygiene an der Universität Rostock. Ob die Impfung auch eine Ansteckung verhindert, ist derzeit unklar. "Wir hoffen natürlich alle, dass die Impfung auch die Infektion verhindert, aber wir wissen es momentan nicht", sagte Thomas Mertens, Vorsitzender der Ständigen Impfkommission (Stiko) am Robert Koch-Institut vor Kurzem der "Frankfurter Allgemeinen Sonntagszeitung". Denkbar ist, dass Geimpfte sich anstecken und das Virus weitergeben, obwohl sie selbst nicht erkranken.
Wie gut schützt der Impfstoff?
Nach den klinischen Studien gibt Biontech die Wirksamkeit des Impfstoffs mit 95 Prozent an. Das bedeutet: Unter den Probanden der geimpften Gruppe traten 95 Prozent weniger Erkrankungen auf als unter den Probanden der Kontrollgruppe.
Ob die genannte - für viele Experten überraschend hohe - Wirksamkeit auch bei einem massenhaften Einsatz des Impfstoffes erreicht wird, wird sich erst in einigen Monaten zeigen. Die Zahlen beziehen sich auf die bisher durchgeführten Phase-III-Studien, wie Virologe Podbielski erklärt. "Jetzt ist unter idealisierten Bedingungen geimpft worden", sagt er. Im Alltagseinsatz sind die Bedingungen nicht immer optimal. Der Impfstoff von Biontech müsse extrem gekühlt werden, nennt Podbielski als Beispiel. Ob eine lückenlose Kühlkette bei den Impfungen weltweit möglich sei, bezweifelt er.
Ein weiteres Problem, das für alle Covid-Impfstoffe gelte: Die Tests würden vor allem bei gesunden Menschen durchgeführt. Das Immunsystem bei älteren Menschen oder Menschen mit Vorerkrankungen wie Diabetes reagiere aber nicht so gut auf Impfungen wie das Immunsystem Gesunder. Insofern kann es Podbielski zufolge passieren, dass die Daten zur Wirksamkeit der Impfstoffe nach Impfung großer Teile der Weltbevölkerung weniger gut ausfallen. Biontech berichtete bei der Vorstellung der ersten Ergebnisse der Phase-III-Studie, keinen Unterschied zwischen verschiedenen Altersgruppen hinsichtlich der Wirksamkeit gefunden zu haben.
Welchen Einfluss haben Virus-Mutationen auf die Wirksamkeit?
Das Erbgut der Coronaviren verändert sich laufend, das ist an sich nicht ungewöhnlich. Die genetischen Veränderungen können auch die Eigenschaften des Virus verändern, etwa dafür sorgen, dass es leichter menschliche Zellen befallen oder den Angriffen der Immunabwehr besser entkommen kann. In Großbritannien kursiert zum Beispiel seit einiger Zeit eine neue Virusvariante, die sich anscheinend deutlich schneller ausbreitet als die bisherigen Varianten. Experten schätzen die Gefahr als gering ein, dass der auch in Großbritannien eingesetzte Impfstoff gegen diese Variante nicht mehr oder schlechter wirkt. Die Immunreaktionen, die der Impfstoff hervorruft, richten sich gegen mehrere Merkmale des Virus, einzelne Mutationen dürften sich deshalb nicht dramatisch auswirken.
Wie lange schützt der Impfstoff?
Auch diese Frage lässt sich noch nicht abschließend beantworten, weil die Studien noch nicht lange genug laufen. Eine kürzlich veröffentlichte US-Untersuchung gibt erste Hinweise. Demnach sind bei Menschen nach einer natürlichen Infektion sowohl Antikörper als auch T-Zellen - zwei der zentralen Waffen unseres Immunsystems - zumindest fünf Monate nach dem Einsetzen der Symptome noch nachweisbar. Das ist selbst bei Verläufen mit milden Symptomen der Fall. Die Studie wurde als sogenanntes Preprint veröffentlicht, ist also bisher nicht von unabhängigen Experten begutachtet worden.
Weitere Studien zeigen, dass man bei anderen Coronaviren als SARS-CoV-2, die normale Erkältungen auslösen, ein bis eineinhalb Jahre vor einer erneuten Infektion geschützt ist. Bei einer Impfung falle die Immunantwort gemeinhin effizienter aus, sagt Carsten Watzl, Immunologe am Leibniz-Institut für Arbeitsforschung der Technischen Universität Dortmund. "Die Hoffnung ist also, dass die Immunität durch die Impfstoffkandidaten deutlich länger anhält."
Welche Nebenwirkungen gibt es beim Impfstoff von Biontech und Pfizer?
Müdigkeit, Kopfweh, Schmerzen an der Einstichstelle gehören zu den häufigsten Nebenwirkungen der Impfung. Solche Begleiterscheinungen sind Impfexperten zufolge üblich. Einer Studie mit 44.820 Teilnehmern zufolge - von denen etwa die Hälfte den Biontech-Impfstoff bekommen hatte - klagten manche außerdem über Fieber, Schüttelfrost, Durchfall oder Muskel- und Gliederschmerzen. Im Allgemeinen waren die Nebenwirkungen schwach bis mäßig und klangen nach kurzer Zeit ab. Im Vergleich zu vielen etablierten Impfstoffen wie etwa dem gegen Grippe traten die Nebenwirkungen aber vergleichsweise häufiger auf. Impfexperten verglichen die Reaktionen mit denen nach Gabe eines Gürtelrose-Impfstoffs.
Vereinzelt gab es bei den Tests "unerwünschte Ereignisse" wie geschwollene Lymphknoten. Je eine Person meldete eine Schulterverletzung, Herzrhythmusstörungen sowie Parästhesie im Bein, also Taubheitsgefühl. Grundsätzlich traten Begleiterscheinungen öfter bei der zweiten Impfdosis auf. Mögliche selten auftretende Nebenwirkungen konnten aufgrund der kurzen Beobachtungszeit noch nicht erfasst werden. Deshalb wird die Verträglichkeit des Impfstoffes auch nach Zulassung weiter geprüft.
Bei den Impfungen in Großbritannien hatten einige Menschen stärkere allergische Reaktionen gezeigt. Aus diesem Grund haben die Behörden veranlasst, Menschen mit größeren Allergieproblemen vorerst nicht zu impfen. Dass das Problem in den klinischen Studien nicht aufkam, liegt ganz einfach daran, dass Menschen mit schweren Allergien gegen Impfstoffe oder Bestandteile davon von der Teilnahme ausgeschlossen waren, erläuterte kürzlich Biontech-Geschäftsvorstand Sean Marett.
Wie wird (wann) geimpft?
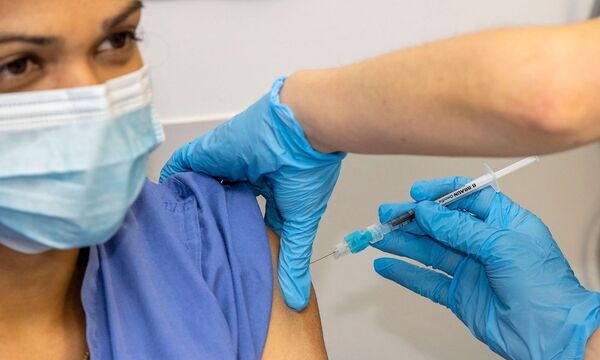
Jeder Patient bekommt zwei Impfdosen im Abstand von drei Wochen, die jeweils in den Oberarm gespritzt werden - genauer gesagt in den Deltamuskel (Musculus deltoideus). "Er könnte im Prinzip in jeden Muskel gespritzt werden, aber die Stelle am Arm ist eben gut zugänglich", sagt Virologe Podbielski. Der Vorteil einer solchen intramuskulären Impfung: Der Wirkstoff bleibt für einige Stunden im Muskel und der Körper hat so Zeit, ihn zu erkennen und darauf zu reagieren.
Die Lieferung von rund 10.000 Impfdosen noch vor Neujahr dürften Wien und Niederösterreich zugutekommen, die erste große Charge - für den Jänner wurden mehr als 240.000 Impfdosen angekündigt - soll dann offenbar nach dem Bevölkerungsschlüssel auf die Bundesländer aufgeteilt werden.
Diese Impfdosen werden entsprechend der österreichischen Impfstrategie in den Alters- und Pflegeheimen zur Anwendung kommen. Die nächste Lieferung erfolgt dann mit 200.000 Dosen vom Hersteller Moderna, über den Zulassung dieses Impfstoffes wird die EMA am 6. Jänner entscheiden.
Impfpflicht: Notwendige Maßnahme oder unzulässiger Zwang? Diskutieren Sie mit!
Damit wird die Immunisierung des Gesundheitspersonals in Krankenhäusern, Ordinationen etc. und von Hochrisikogruppen möglich sein. Die dritte Impfstofftranche sollte von AstraZeneca kommen und ist mit rund zwei Millionen Vakzin-Dosen die höchste. Damit wird die zweite Impfplan-Phase eingeleitet: Impfungen für alle Personen über 65 sowie solche mit Systemrisiko in den Bereichen Bildung, Sicherheit, Justiz und in der kritischen Infrastruktur. Ab Sommer folgt dann der Rest der Bevölkerung.
Wo der Impfstoff schon im Einsatz ist
Die Schweiz hat dem vom deutschen Unternehmen Biontech und dessen US-Partner Pfizer entwickelten Corona- Impfstoff unterdessen bereits die Zulassung erteilt. Es handelt sich um die weltweit erste Zulassung in einem ordentlichen Verfahren und nicht im Zuge einer Notfallzulassung. Der Impfstoff sei seit Mitte Oktober bei laufend eingereichten Unterlagen begutachtet worden, teilte die Zulassungsbehörde Swissmedic am Samstag in Bern mit.
Das Vakzin ist seit Anfang Dezember in Großbritannien im Einsatz. Auch die USA, Kanada, Bahrain, Saudiarabien, Mexiko, Ecuador und Chile haben mittlerweile den Impfstoff genehmigt. Die europäische Arzneimittelagentur EMA gibt am Montag ihre Beurteilung ab. Fällt sie positiv aus, könnte in der EU ab 27. Dezember geimpft werden.
In den USA wurde indes bereits der zweite Corona-Impfstoff zugelassen. Die Arzneimittelbehörde FDA erteilte am Freitag die – bislang weltweit erste – Notfallgenehmigung für das Vakzin des US-Pharma-Unternehmens Moderna. Anfang kommender Woche kann laut Regierungsbeamten mit dem Einsatz des Präparats begonnen werden. „Gratulation, der Moderna-Impfstoff ist jetzt verfügbar“, twitterte US-Präsident Donald Trump wenige Minuten nach der Erklärung der FDA.
(APA/AFP/dpa/Red.)